NIPT標(biāo)準(zhǔn)品-助力無創(chuàng)產(chǎn)前檢測(cè)
發(fā)布時(shí)間:2024/01/25分類:技術(shù)文章來源:科佰生物
01
背景
無創(chuàng)產(chǎn)前診斷技術(shù)(noninvasive prenatal testing,NIPT)主要是利用NGS方法檢測(cè)孕婦的外周血游離DNA(游離DNA指血漿中自然條件下已經(jīng)片段化的DNA)檢測(cè)胎兒是否存在染色體非整數(shù)倍異常。常見的染色體疾病包括常染色體非整倍體異常、 性染色體非整倍體異常、 染色體拷貝數(shù)變異等。少數(shù)染色體畸變者能存活至出生,常造成機(jī)體多發(fā)畸形、智力低下、生長(zhǎng)發(fā)育遲緩和多系統(tǒng)功能障礙。目前, 產(chǎn)前篩查及產(chǎn)前診斷是避免致死致殘性染色體疾病患兒出生的前提及主要措施。
常見的篩查方法
常見的篩查染色體異常的方法有G顯帶,熒光原位雜交(FISH),DNA微陣列(CMA),NIPT,NIPT-Plus,CNV-seq等。
染色體核型分析(G顯帶)一般用來檢測(cè)染色體的數(shù)目和大結(jié)構(gòu)異常,是檢測(cè)的金標(biāo)準(zhǔn)。FISH理論上可以檢測(cè)基因組中任何位置的信息,但是需要相應(yīng)的探針。目前臨床常用的就是13,18,21染色體以及性染色體的檢測(cè)試劑盒。NIPT和 NIPT- Plus是基于NGS方法的檢測(cè)手段,NIPT后續(xù)通過Z scores判斷染色體是否異常。而單基因病無創(chuàng)產(chǎn)前檢測(cè)是針對(duì)單基因遺傳病。DNA微陣列主要是檢測(cè)染色體的微缺失和微重復(fù),通過log R ratio判斷是否異常。
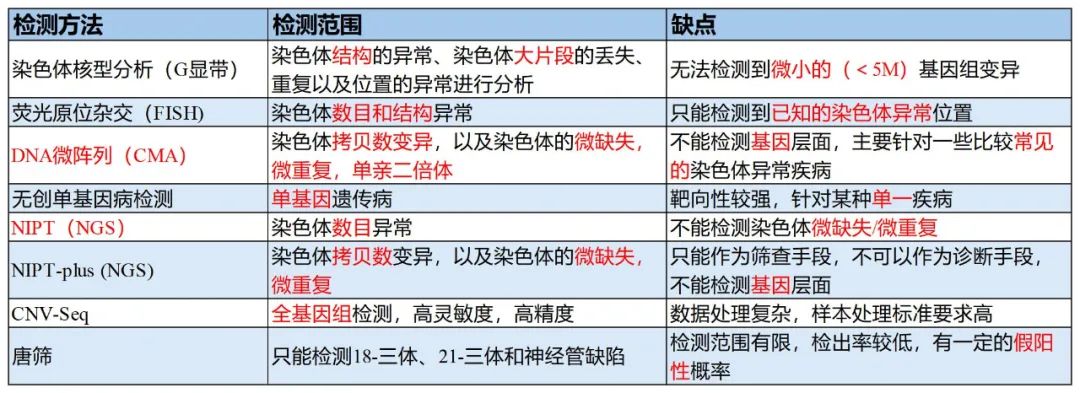
Table 1. 常見染色體檢測(cè)方法的比較
科佰生物
在檢測(cè)的過程中,質(zhì)控品和參考品是必不可少的。針對(duì)NIPT檢測(cè),科佰推出染色體非整倍數(shù)參考品和質(zhì)控品,包含常染色體和性染色體,以及微缺失和微重復(fù)質(zhì)控品和參考品,后期還將陸續(xù)推出嵌合體的參考品。

部分產(chǎn)品數(shù)據(jù)展示
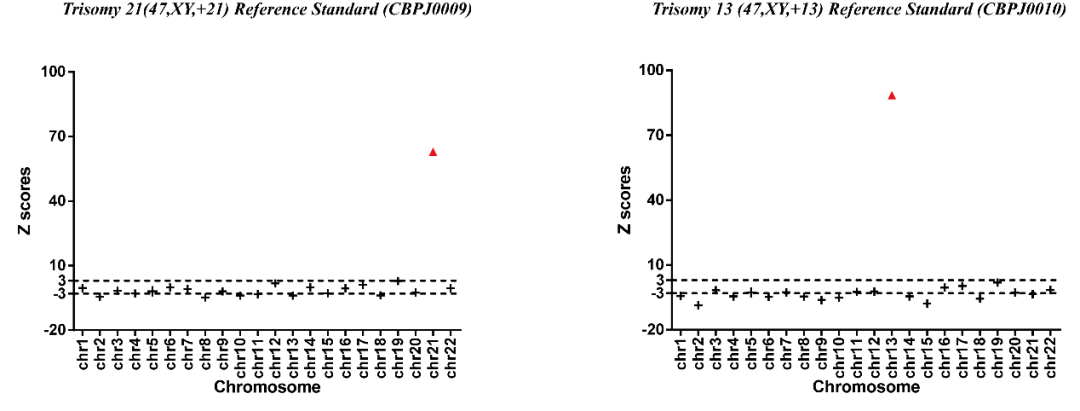
Fig 1. Results of NGS with Trisomy 21 (47,XY,+21) Reference Standard and Trisomy 13 (47,XY,+13) Reference Standard.
NGS技術(shù)可對(duì)cfDNA進(jìn)行測(cè)序,結(jié)合信息分析方法,通過Z scores評(píng)估胎兒染色體非整倍性的風(fēng)險(xiǎn)率。當(dāng)Z scores >3或者<-3時(shí),判定該染色體異常。Z scores >3判定該染色體存在重復(fù),Z scores<-3判定該染色體存在缺失。
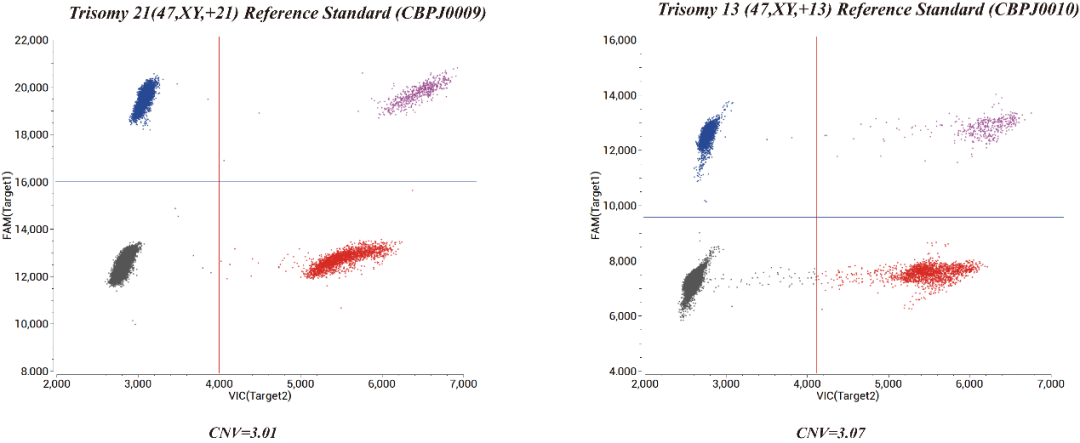
Fig 2. Results of ddPCR with Trisomy 21 (47,XY,+21) Reference Standard and Trisomy 13 (47,XY,+13) Reference Standard.
根據(jù)NGS結(jié)果確定異常染色體后,依據(jù)人基因組序列設(shè)計(jì)相關(guān)異常染色體的引物和探針,ddPCR方法再次驗(yàn)證,通過CNV值判斷染色體情況(默認(rèn)整條染色體每間隔一段距離選擇一段擴(kuò)增區(qū)域)。
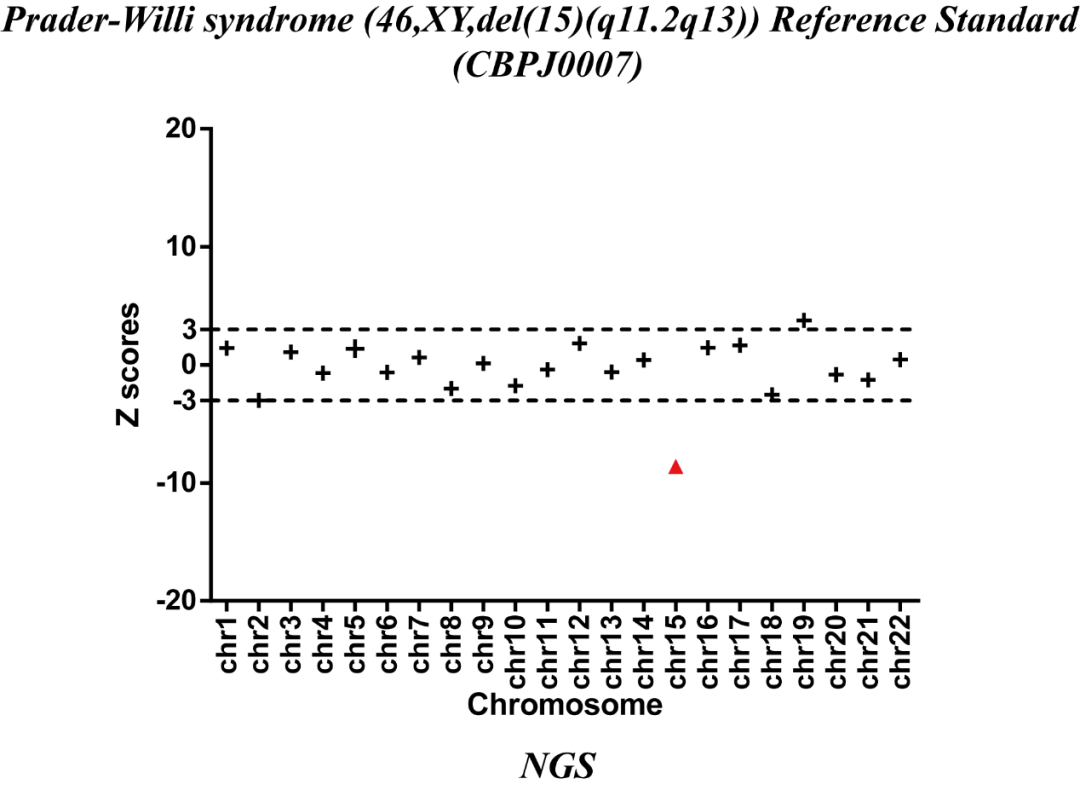
Fig 3. Results of NGS with Prader-Willi syndrome (46,XY,del(15)(q11.2q13)) Reference Standard.
微缺失和微重復(fù)質(zhì)控品和參考品通過NGS和CMA方法驗(yàn)證。通過NGS可以確定15號(hào)染色體發(fā)生缺失,CMA方法可以判斷樣本微缺失區(qū)域?yàn)?/span>15q11.2q13。根據(jù)上述驗(yàn)證方法明確缺失或重復(fù)區(qū)域后,根據(jù)缺失或者重復(fù)的區(qū)域設(shè)計(jì)引物和探針,進(jìn)行ddPCR檢測(cè),再次驗(yàn)證樣本的異常情況。
所有樣本后期均通過酶切或超聲的方式模擬臨床樣本,將DNA進(jìn)行片段化處理后,通過ddPCR技術(shù)對(duì)參考品進(jìn)行準(zhǔn)確定標(biāo),準(zhǔn)確檢測(cè)參考品中胎兒游離DNA占比。將經(jīng)過ddPCR檢測(cè)過的樣本混入無DNA的血漿中,更接近臨床樣本。
科佰推出的NIPT系列參考品不僅可以適用于多種檢測(cè)方法,還可以用于評(píng)價(jià)高通量測(cè)序法判定的胎兒游離DNA濃度是否準(zhǔn)確。